ĐÁNH GIÁ NHỎ
Tiền đồn chống lại ung thư: các dấu hiệu ung thư phổ quát
Chengchen Qian1, Xiaolong Zou2, Wei Li1,3, Yinshan Li4, Wenqiang Yu5
1Công ty TNHH Công nghệ sinh học Epiprobe Thượng Hải, Thượng Hải 200233, Trung Quốc;2 Khoa Ngoại tổng hợp, Bệnh viện trực thuộc số 1 của Đại học Y Cáp Nhĩ Tân, Cáp Nhĩ Tân 150001, Trung Quốc;3Shandong Epiprobe Medical Laboratory Co., Ltd, Heze 274108, Trung Quốc;Bệnh viện Nhân dân số 4 Khu tự trị Ninh Hạ Hui, Đại học Y Ninh Hạ, Ngân Xuyên 750002, Trung Quốc;5Trung tâm Lâm sàng Y tế Công cộng Thượng Hải & Khoa Phẫu thuật Tổng quát, Bệnh viện Huashan & Viện Di căn Ung thư & Phòng thí nghiệm Biểu sinh RNA, Viện Khoa học Y sinh, Đại học Y Thượng Hải, Đại học Phúc Đán, Thượng Hải 200032, Trung Quốc
TRỪU TƯỢNG
Ung thư là nguyên nhân gây tử vong hàng đầu trên toàn thế giới.Phát hiện sớm ung thư có thể làm giảm tỷ lệ tử vong của tất cả các loại ung thư;tuy nhiên, hầu hết các loại ung thư đều thiếu các dấu ấn sinh học phát hiện sớm hiệu quả.Quá trình methyl hóa DNA luôn là mục tiêu được quan tâm chính vì quá trình methyl hóa DNA thường xảy ra trước những thay đổi di truyền khác có thể phát hiện được.Trong khi nghiên cứu các đặc điểm chung của bệnh ung thư bằng cách sử dụng trình tự định vị hướng dẫn mới để methyl hóa DNA, một loạt các dấu hiệu chỉ ung thư phổ quát (UCOM) đã nổi lên như những ứng cử viên nặng ký để phát hiện sớm ung thư một cách hiệu quả và chính xác.Mặc dù giá trị lâm sàng của các dấu ấn sinh học ung thư hiện tại bị giảm đi do độ nhạy thấp và/hoặc độ đặc hiệu thấp, nhưng các đặc điểm độc đáo của UCOM đảm bảo kết quả có ý nghĩa lâm sàng.Việc xác nhận tiềm năng lâm sàng của UCOM trong ung thư phổi, cổ tử cung, nội mạc tử cung và tiết niệu hỗ trợ thêm cho việc áp dụng UCOM trong nhiều loại ung thư và các tình huống lâm sàng khác nhau.Trên thực tế, các ứng dụng của UCOM hiện đang được nghiên cứu tích cực với đánh giá sâu hơn trong việc phát hiện sớm ung thư, chẩn đoán phụ trợ, hiệu quả điều trị và theo dõi tái phát.Các cơ chế phân tử mà UCOM sử dụng để phát hiện ung thư là chủ đề quan trọng tiếp theo cần được nghiên cứu.Việc áp dụng UCOM trong các tình huống thực tế cũng đòi hỏi phải triển khai và sàng lọc.
TỪ KHÓA
Phát hiện ung thư;sàng lọc ung thư;Quá trình methyl hóa DNA;biểu sinh ung thư;dấu ấn sinh học ung thư
Tại sao chúng ta cần gấp cái mới dấu ấn sinh học?
Sau hơn một thế kỷ chiến đấu với ung thư, ung thư vẫn là mối đe dọa sinh học nguy hiểm nhất đối với nhân loại.Ung thư vẫn là mối lo ngại về sức khỏe toàn cầu với 19,3 triệu ca mắc mới và gần 10 triệu ca tử vong ước tính vào năm 20201. Năm 2020, ước tính có 4,6 triệu ca ung thư mới được chẩn đoán ở Trung Quốc, chiếm 23,7% số ca ung thư mới trên toàn cầu theo GLOBOCAN1.Hơn nữa, khoảng 3 triệu ca tử vong được cho là do ung thư ở Trung Quốc vào năm 2020, chiếm 30% số ca tử vong liên quan đến ung thư trên toàn cầu1.Những thống kê này chỉ ra rằng Trung Quốc đứng đầu về tỷ lệ mắc và tử vong do ung thư.Hơn nữa, tỷ lệ sống sót sau 5 năm ung thư là 40,5%, thấp hơn 1,5 lần so với tỷ lệ sống sót sau 5 năm ở Hoa Kỳ2,3.Tỷ lệ sống sót tương đối thấp hơn và tỷ lệ tử vong cao hơn ở Trung Quốc so với các nước có chỉ số phát triển con người cao hơn cho thấy rằng một hệ thống giám sát và ngăn ngừa ung thư hiệu quả và tiết kiệm chi phí là rất cần thiết.Phát hiện sớm ung thư là một trong những yếu tố quan trọng nhất trong hệ thống chăm sóc sức khỏe.Phát hiện sớm ung thư có thể cải thiện tiên lượng và khả năng sống sót ở giai đoạn đầu ở hầu hết các loại ung thư4.Các chiến lược sàng lọc thành công đã làm giảm đáng kể tỷ lệ mắc và tỷ lệ tử vong của ung thư cổ tử cung, vú, đại trực tràng và tuyến tiền liệt.
Tuy nhiên, để phát hiện sớm bệnh ung thư không phải là điều dễ dàng.Điều tra sinh học và tiên lượng bệnh ung thư giai đoạn đầu, xác định và xác nhận các dấu hiệu sinh học phát hiện sớm đáng tin cậy cũng như phát triển các công nghệ phát hiện sớm chính xác và dễ tiếp cận luôn là những trở ngại lớn nhất trong quá trình4.Việc phát hiện chính xác ung thư có thể phân biệt các tổn thương lành tính với ác tính, giúp tránh các thủ tục không cần thiết và tạo điều kiện quản lý bệnh tốt hơn.Các chiến lược phát hiện sớm hiện nay bao gồm sinh thiết dựa trên nội soi, hình ảnh y tế, tế bào học, xét nghiệm miễn dịch và xét nghiệm dấu ấn sinh học5-7.Là phương pháp xâm lấn và tốn kém, sinh thiết dựa trên nội soi mang một gánh nặng vốn có vì đây là một thủ tục y tế lớn phụ thuộc vào nhân viên chuyên môn.Giống như tế bào học, cả hai phương pháp sàng lọc đều phụ thuộc vào các chuyên gia y tế và dựa trên đánh giá cá nhân với kết quả không đạt mức lý tưởng8.Ngược lại, xét nghiệm miễn dịch có độ chính xác cao, do tỷ lệ dương tính giả cao.Hình ảnh y tế, như một chiến thuật sàng lọc, đòi hỏi thiết bị đắt tiền và kỹ thuật viên chuyên môn.Do đó, hình ảnh y tế rất hạn chế do khả năng tiếp cận thấp.Vì tất cả những lý do này, dấu ấn sinh học dường như là lựa chọn tốt hơn để phát hiện sớm ung thư.
Thư từ: Yinshan Li và Wenqiang Yu
Email: liyinshan@nxrmyy.com and wenqiangyu@fudan.edu.cn
ID ORCID: https://orcid.org/0009-0005-3340-6802 và
https://orcid.org/0000-0001-9920-1133
Nhận ngày 22 tháng 8 năm 2023;chấp nhận ngày 12 tháng 10 năm 2023;
được xuất bản trực tuyến ngày 28 tháng 11 năm 2023.
Có sẵn tại www.cancerbiomed.org
©2023 Sinh học & Y học Ung thư.Commons sáng tạo
Giấy phép Quốc tế Ghi công-Phi Thương mại 4.0
Dấu ấn sinh học hiện được phân loại là protein, dấu hiệu đột biến DNA, dấu hiệu biểu sinh, bất thường nhiễm sắc thể, dấu hiệu RNA có nguồn gốc trực tiếp từ khối u hoặc các mảnh khối u thu được gián tiếp từ dịch cơ thể.Dấu hiệu protein là dấu ấn sinh học được ứng dụng rộng rãi nhất trong sàng lọc và chẩn đoán ung thư.Các dấu ấn sinh học protein, như các dấu hiệu sinh học sàng lọc, bị hạn chế do xu hướng bị ảnh hưởng bởi các tổn thương lành tính, dẫn đến chẩn đoán quá mức và điều trị quá mức, như đã được báo cáo đối với α-fetoprotein và kháng nguyên đặc hiệu tuyến tiền liệt (PSA)9,10.Các dấu hiệu RNA bao gồm các mẫu biểu hiện di truyền và các dấu hiệu RNA không mã hóa khác. Sự kết hợp của các dấu hiệu RNA biểu hiện di truyền có thể được phát hiện bằng cách sử dụng các mẫu nước tiểu, độ nhạy của chúng không đạt yêu cầu (60%) đối với các khối u nguyên phát và việc phát hiện chúng có thể bị ảnh hưởng bởi tính chất phân hủy dễ dàng của RNA trong môi trường bình thường11.Các dấu hiệu di truyền và biểu sinh đều phải đối mặt với vấn đề về tỷ lệ phổ biến ở các khối u và hạn chế đối với các loại ung thư.
Quá trình methyl hóa DNA là một ứng cử viên sáng giá như một dấu ấn sinh học phát hiện sớm kể từ khi được Feinberg liên kết lần đầu tiên với bệnh ung thư vào năm 198312. Sự sai lệch methyl hóa DNA được quan sát thấy ở tất cả các giai đoạn của bệnh ung thư, ngay từ giai đoạn tiền ung thư.Quá trình tăng cường DNA bất thường thường diễn ra trên các đảo CpG trong các chất kích thích gen để chống lại các chất ức chế khối u13,14.Các nghiên cứu cũng gợi ý rằng quá trình methyl hóa DNA bất thường có liên quan đến việc điều hòa lại các cơ quan điều chỉnh phát triển15.Thung lũng methyl hóa DNA, thường liên quan đến các chất điều hòa phát triển và ung thư tăng methyl, có thể chuyển chế độ biểu hiện gen sang chế độ phụ thuộc vào quá trình methyl hóa DNA ổn định hơn và giảm kết nối với histone H3K27me3 bị methyl hóa và các protein polycomb liên quan16,17.
Trong số lượng lớn các dấu hiệu methyl hóa DNA được công bố, một số đã ra mắt thành công trên thị trường;tuy nhiên, các dấu hiệu và bảng chẩn đoán methyl hóa DNA được thương mại hóa hiện nay vẫn chưa phát huy hết tiềm năng phát hiện sớm ung thư vì nhiều lý do18.Mặc dù hầu hết đều cho thấy hiệu suất chấp nhận được khi sử dụng thông tin cơ sở dữ liệu, nhưng các dấu ấn sinh học này thường hoạt động kém lý tưởng hơn trong thế giới thực do thực tế là các mẫu trong thế giới thực thường phức tạp hơn và không mang tính đại diện như các mẫu được chọn trong cơ sở dữ liệu.Việc phát hiện sớm quá trình methyl hóa đa ung thư dựa trên trình tự thế hệ tiếp theo đã được chứng minh là có độ nhạy tương ứng chỉ là 16,8% và 40,4% ở ung thư giai đoạn I và II19.Các xét nghiệm phát hiện sớm đòi hỏi độ ổn định cao hơn và dấu ấn sinh học chính xác hơn.
Phát hiện dấu hiệu ung thư phổ quát (UCOM) bằng cách sử dụng trình tự định vị hướng dẫn (GPS)
Mặc dù đã có nhiều thập kỷ nghiên cứu về ung thư nhưng việc phòng ngừa và điều trị thỏa đáng vẫn chưa được thực hiện.Các phương pháp mới là cần thiết để cho phép các nhà nghiên cứu đánh giá kỹ lưỡng về bệnh ung thư.Trong 23 năm qua, 6 dấu hiệu ung thư, như trốn tránh apoptosis, xâm lấn mô và di căn, v.v., đã được mở rộng lên 14 bằng cách bao gồm các đặc điểm như lập trình lại biểu sinh không đột biến và hệ vi sinh vật đa hình20,21.Khi nhiều chi tiết liên quan đến ung thư được tiết lộ, nhiều góc nhìn hơn được đưa vào nghiên cứu ung thư.Nghiên cứu về ung thư dần bước sang một thời kỳ mới theo hai hướng (chung và cá nhân).Với sự phát triển của ung thư chính xác trong những năm gần đây, trọng tâm của nghiên cứu ung thư đang nghiêng về liệu pháp nhắm mục tiêu cá nhân hóa và tính không đồng nhất của bệnh ung thư22.Do đó, các dấu ấn sinh học ung thư được xác định gần đây đã tập trung chủ yếu vào các loại ung thư cụ thể, chẳng hạn như ung thư cưỡng bức PAX6 và BMP3 đối với ung thư đại trực tràng24.Hiệu suất của các dấu ấn sinh học đặc trưng cho các loại ung thư này khác nhau, nhưng những người nhạy cảm vẫn không thể sàng lọc đồng thời tất cả các bệnh ung thư do hạn chế thu thập mẫu sinh học và chi phí cao.Sẽ thật lý tưởng nếu chúng ta có thể xác định được một dấu ấn sinh học mạnh mẽ, duy nhất có hiệu quả đối với tất cả các loại ung thư ở giai đoạn đầu.
Để đạt được mục tiêu lý tưởng như vậy, phải chọn một ứng cử viên dấu ấn sinh học tốt hơn từ danh sách các loại dấu ấn sinh học tiềm năng.Những sai lệch methyl hóa DNA, trong số tất cả các cấu hình di truyền và biểu sinh, được biết là có liên quan đến ung thư và là một trong những bất thường sớm nhất, nếu không phải là đầu tiên, liên quan đến ung thư xảy ra theo trình tự thời gian.Việc điều tra quá trình methyl hóa DNA đã bắt đầu sớm nhưng bị cản trở do thiếu phương pháp nghiên cứu.Trong số 28 triệu vị trí CpG bị methyl hóa tiềm năng trong bộ gen, một số lượng có thể quản lý được phải được phát hiện và liên kết với bộ gen để hiểu rõ hơn về nguyên nhân khối u.Giải trình tự bisulfite toàn bộ bộ gen (WGBS), được coi là tiêu chuẩn vàng của giải trình tự methyl hóa DNA, chỉ có thể bao phủ 50% C trong tế bào ung thư do bản chất của việc xử lý bằng bisulfite làm phá vỡ các đoạn DNA và làm giảm độ phức tạp của bộ gen trong quá trình xử lý. sự chuyển đổi Cs-to-Ts25.Các phương pháp khác, chẳng hạn như chip 450k, chỉ xử lý được 1,6% quá trình methyl hóa bộ gen.Dựa trên dữ liệu 450k, bảng phát hiện methyl hóa DNA có độ nhạy 35,4% đối với 6 loại ung thư giai đoạn I26.Những hạn chế của các loại ung thư, hiệu suất kém và tiếng ồn do các phương pháp phát hiện trong quá trình phân tích tạo ra đã trở thành trở ngại lớn nhất đối với các bảng phát hiện ung thư toàn thể.
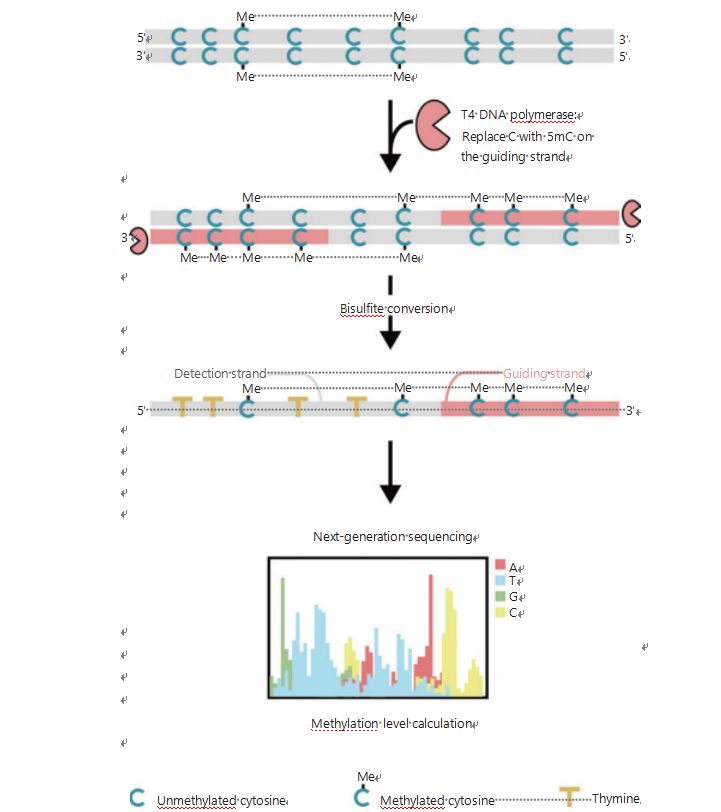
Để nghiên cứu tốt hơn các kiểu biểu sinh của tế bào trong quá trình hình thành khối u và di căn, chúng tôi đã phát triển một GPS duy nhất để phát hiện quá trình methyl hóa DNA trên toàn bộ gen, bao phủ tới 96% vị trí CpG trong 0,4 tỷ lượt đọc25.GPS là phương pháp giải trình tự song phương sử dụng đoạn DNA đầu 3’ của methyl-cytosine không chuyển đổi được sau khi xử lý bằng bisulfite để hướng dẫn việc căn chỉnh tính toán methyl hóa DNA của đầu 5’ thông qua trình tự đầu cặp (Hình 1)25.Chuỗi dẫn hướng methyl-cytosine, hoạt động như một chuỗi mẫu, hỗ trợ việc căn chỉnh vùng có GC cao giúp khôi phục dữ liệu giải trình tự bị bỏ quên nhiều nhất trong WGBS truyền thống.Tính năng bao phủ cao của GPS cung cấp một lượng lớn thông tin methyl hóa DNA, cho phép chúng tôi kiểm tra hồ sơ methyl hóa ung thư với độ phân giải cao hơn đáng kể ở các khu vực chưa được nghiên cứu trước đây.
GPS cung cấp cho chúng ta một công cụ mạnh mẽ để nghiên cứu tính đồng nhất của bệnh ung thư, điều này có thể đơn giản hóa đáng kể việc nghiên cứu ung thư và có khả năng tìm ra lời giải thích phổ quát cho nguyên nhân khối u và di căn.Trong khi phân tích dữ liệu GPS của các dòng tế bào ung thư, người ta thường xuyên gặp phải một hiện tượng đặc biệt.Có một số vùng dường như bị tăng methyl hóa bất thường trong nhiều loại mẫu ung thư.Phát hiện bất ngờ này sau đó đã được xác nhận để phục vụ như UCOM.Hơn 7.000 mẫu từ 17 loại ung thư trong cơ sở dữ liệu The Cancer Genome Atlas (TCGA) đã được phân tích, trong đó chúng tôi đã xác định được UCOM đầu tiên, HIST1H4F, một gen liên quan đến histone bị tăng methyl hóa trong tất cả các loại ung thư27.Sau đó, một loạt UCOM đã được tìm thấy và xác nhận trong cơ sở dữ liệu TCGA, cơ sở dữ liệu Gene Expression Omnibus (GEO) và các mẫu lâm sàng trong thế giới thực.Tính đến thời điểm hiện tại, HIST1H4F, PCDHGB7 và SIX6 đã được tìm thấy và xác nhận là UCOM.Phát hiện bất ngờ về UCOM đưa ra câu trả lời mạnh mẽ cho nhu cầu phát hiện sớm bệnh ung thư.UCOM cung cấp giải pháp phát hiện một dấu hiệu của nhiều bệnh ung thư.
Đặc điểm của UCOM
Sau khi xác nhận, UCOM đã được chứng minh là thể hiện bốn đặc điểm chính cho phép UCOM vượt qua hiệu quả của các dấu ấn sinh học hiện tại (Hình 2).
Độc nhất đối với bệnh ác tính
UCOM chỉ dành riêng cho các tổn thương ung thư hoặc tiền ung thư và không bị ảnh hưởng bởi những thay đổi sinh lý bình thường.Một số dấu hiệu liên quan đến ung thư hiện nay được áp dụng rộng rãi trong việc phát hiện và/hoặc sàng lọc sớm đã dẫn đến chẩn đoán quá mức.Mức PSA tăng cao, một công cụ sàng lọc được công nhận về mặt lâm sàng, cũng được phát hiện trong các tình trạng lành tính, chẳng hạn như tăng sản tuyến tiền liệt và viêm tuyến tiền liệt10.Việc chẩn đoán quá mức và điều trị quá mức dẫn đến giảm chất lượng cuộc sống do các biến chứng về ruột, tiết niệu và tình dục28.Các dấu ấn sinh học dựa trên protein và được sử dụng rộng rãi khác trong môi trường lâm sàng, chẳng hạn như CA-125, không mang lại lợi ích đáng kể nào trong khi gây ra tình trạng chẩn đoán quá mức và điều trị quá mức29.Độ đặc hiệu cao của UCOM đối với các khối u ác tính tránh được những thiếu sót này.UCOM, PCDHGB7, phân biệt hiệu quả các tổn thương nội biểu mô vảy cấp độ cao (HSIL) và ung thư cổ tử cung với các mẫu bình thường và các tổn thương nội mô vảy cấp độ thấp (LSIL), trong khi hầu hết các dấu hiệu sinh học khác chỉ có thể phân biệt ung thư cổ tử cung với các mẫu bình thường30.Mặc dù PCDHGB7 không phát hiện sự khác biệt đáng kể giữa nội mạc tử cung bình thường và tăng sản nội mạc tử cung, nhưng sự khác biệt đáng kể được phát hiện giữa nội mạc tử cung bình thường và tăng sản không điển hình, và thậm chí còn có sự khác biệt lớn hơn giữa nội mạc tử cung bình thường và ung thư nội mạc tử cung (EC) dựa trên PCDHGB731.UCOM là duy nhất cho các tổn thương ác tính trong cơ sở dữ liệu và mẫu lâm sàng.Từ quan điểm của bệnh nhân, các UCOM độc đáo làm giảm ngưỡng hiểu các chỉ dẫn phức tạp của nhiều dấu ấn sinh học không ổn định hoạt động kém và sự lo lắng tương ứng trong quá trình đánh giá.Từ quan điểm của bác sĩ lâm sàng, các UCOM độc đáo giúp phân biệt khối u ác tính với các tổn thương lành tính, hỗ trợ phân loại bệnh nhân và giảm các thủ tục y tế không cần thiết cũng như điều trị quá mức.Do đó, UCOM độc đáo làm giảm sự dư thừa của hệ thống y tế, giảm bớt sự cố hệ thống và cung cấp nhiều nguồn lực y tế hơn cho những người có nhu cầu.
Hình 1 Sơ đồ quy trình làm việc của GPS để phát hiện quá trình methyl hóa DNA25.Đường màu xám: chuỗi DNA đầu vào;vạch màu đỏ: DNA được xử lý bằng T4 DNA polymerase, thay thế cytosine bằng 5′-methylcytosine ở đầu 3′ của đầu vào;màu xanh C với Me: cytosine bị methyl hóa;màu xanh C: cytosine không được methyl hóa;T màu vàng: thymine25.
Tất cả hoặc không có gì
UCOM chỉ hiện diện trong tế bào ung thư và được phát hiện ổn định ở hầu hết các tế bào ung thư.HIST1H4F đã được xác nhận là có khả năng tăng methyl hóa ở hầu hết các loại khối u nhưng không có trong các mẫu bình thường27.Tương tự, PCDHGB7 và SIX6 cũng đã được chứng minh là có mức độ methyl hóa cao trong tất cả các mẫu khối u nhưng không có trong các mẫu bình thường30-32.Đặc tính độc đáo này cải thiện đáng kể hiệu suất của UCOM về giới hạn phát hiện và độ nhạy.Chỉ có 2% tế bào ung thư có thể được phân biệt trong các mẫu, làm cho UCOM trở thành một dấu ấn sinh học nhạy cảm hơn nhiều so với hầu hết các dấu ấn sinh học hiện có. Là một dấu ấn sinh học được sử dụng để phát hiện ung thư đại trực tràng, đột biến KRAS chỉ tồn tại trong khoảng 36% trường hợp ung thư đại trực tràng, gợi ý khả năng chẩn đoán kém33.Tỷ lệ đột biến KRAS thấp trong ung thư đại trực tràng hạn chế KRAS kết hợp với các dấu ấn sinh học khác.Trên thực tế, sự kết hợp của các dấu ấn sinh học ban đầu có vẻ hứa hẹn nhưng không phải lúc nào cũng tạo ra kết quả khả quan trong khi có độ nhiễu lớn hơn nhiều trong phân tích phát hiện và thường bao gồm các quy trình thí nghiệm phức tạp hơn.Ngược lại, PCDHGB7 và các UCOM khác tồn tại trong tất cả các bệnh ung thư.UCOM phát hiện các thành phần ung thư trong các loại mẫu ung thư khác nhau với độ chính xác tối đa đồng thời loại bỏ các quy trình phân tích khử tiếng ồn phức tạp.Việc phát hiện ung thư trong một mẫu dồi dào không khó, nhưng việc phát hiện ung thư trong một mẫu nhỏ là vô cùng khó khăn.UCOM có khả năng phát hiện một lượng nhỏ bệnh ung thư.
Hình 2 Đặc điểm của UCOM.
Phát hiện ung thư trước những thay đổi bệnh lý
UCOM có thể được phát hiện ở giai đoạn tiền ung thư trước khi có những thay đổi bệnh lý.Là dấu ấn sinh học biểu sinh, các bất thường UCOM xảy ra ở giai đoạn sớm hơn so với các bất thường về kiểu hình và có thể được phát hiện trong suốt quá trình tạo khối u, tiến triển và di căn34,35.Độ nhạy của UCOM theo thời gian giúp nâng cao hiệu suất của UCOM trong việc phát hiện ung thư giai đoạn đầu và các tổn thương tiền ung thư.Việc phát hiện ung thư sớm dựa trên sinh thiết và tế bào học có thể khó khăn ngay cả đối với những nhà giải phẫu bệnh có kinh nghiệm nhất.Một sinh thiết duy nhất thu được qua soi cổ tử cung đã được báo cáo là dương tính ở 60,6% mẫu HSIL+.Cần phải sinh thiết thêm đối với nhiều tổn thương để tăng độ nhạy36.Ngược lại, UCOM, PCDHGB7, có độ nhạy 82% đối với các mẫu HSIL+, vượt qua độ nhạy của sinh thiết và hầu hết các dấu ấn sinh học30.Dấu hiệu methyl hóa, FAM19A4, có độ nhạy 69% đối với CIN2+, tương tự như tế bào học, nhưng không thể phân biệt CIN1 với các mẫu bình thường37.UCOM đã được chứng minh là dấu ấn sinh học phát hiện sớm nhạy cảm hơn nhiều.So với các nhà nghiên cứu bệnh học dựa trên kinh nghiệm, UCOM có độ nhạy phát hiện vượt trội đối với bệnh ung thư giai đoạn đầu, từ đó góp phần cải thiện tiên lượng và khả năng sống sót của bệnh ung thư30.Ngoài ra, UCOM cung cấp một nền tảng phát hiện có thể truy cập được ở những khu vực thiếu các nhà nghiên cứu bệnh học có kinh nghiệm và cải thiện đáng kể hiệu quả phát hiện.Với quy trình lấy mẫu và phát hiện thống nhất, phát hiện UCOM mang lại kết quả ổn định và dễ giải thích, phù hợp hơn với quy trình sàng lọc đòi hỏi ít nhân viên chuyên môn và nguồn lực y tế hơn.
Dễ dàng phát hiện
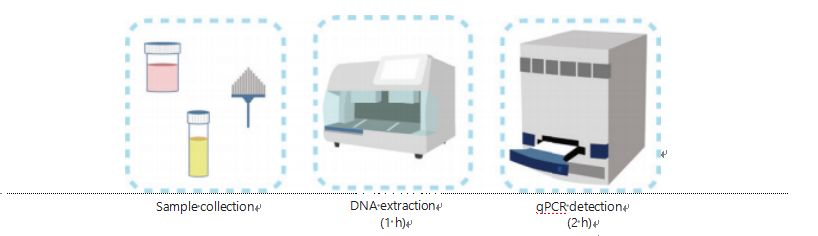
Các phương pháp hiện nay để phát hiện quá trình methyl hóa DNA rất phức tạp và tốn thời gian.Hầu hết các phương pháp đều yêu cầu chuyển hóa bisulfite, gây giảm chất lượng mẫu và có thể tạo ra kết quả không ổn định và không chính xác.Khả năng tái lập kém do xử lý bằng bisulfite có thể dẫn đến sự nhầm lẫn cho bác sĩ và bệnh nhân và gây trở ngại thêm cho các chiến lược theo dõi và/hoặc điều trị.Do đó, chúng tôi đã sửa đổi thêm phương pháp phát hiện UCOM để tránh việc xử lý mẫu bằng bisulfite có vấn đề, đáp ứng các yêu cầu ứng dụng lâm sàng và nâng cao khả năng tiếp cận.Chúng tôi đã phát triển một phương pháp mới sử dụng các enzyme hạn chế nhạy cảm với quá trình methyl hóa kết hợp với PCR định lượng huỳnh quang thời gian thực (Me-qPCR) để định lượng trạng thái methyl hóa của UCOM trong vòng 3 giờ bằng cách sử dụng quy trình xử lý dễ dàng (Hình 3).Me-qPCR có thể chứa nhiều loại mẫu, chẳng hạn như lấy mẫu dịch cơ thể lâm sàng và mẫu nước tiểu tự thu thập.Các mẫu lâm sàng được thu thập có thể được xử lý, lưu trữ và dễ dàng tiến hành phát hiện bằng cách sử dụng phương pháp trích xuất DNA tự động và tiêu chuẩn hóa.Sau đó, DNA được chiết xuất có thể được áp dụng trực tiếp vào nền tảng Me-qPCR để có kết quả định lượng đầu ra và phản ứng một bình.Sau khi phân tích kết quả đơn giản bằng cách sử dụng các mô hình chẩn đoán được trang bị và xác nhận cho các loại ung thư cụ thể, quyết định cuối cùng về kết quả phát hiện UCOM được diễn giải và trình bày dưới dạng giá trị bán định lượng.Nền tảng Me-qPCR vượt trội hơn so với phương pháp giải trình tự bisulfite-pyro truyền thống trong phát hiện UCOM đồng thời tiết kiệm 3 giờ chuyển đổi bisulfite, theo giao thức của bộ EZ DNA Methylation-Gold.Nền tảng phát hiện quá trình methyl hóa cải tiến giúp phát hiện UCOM ổn định hơn, chính xác hơn và dễ tiếp cận hơn30.
Hình 3 Quá trình phát hiện UCOM.Các loại mẫu bao gồm BALF lấy mẫu chuyên nghiệp, bàn chải Pap và/hoặc nước tiểu tự lấy.Quá trình trích xuất DNA có thể được thực hiện bằng máy trích xuất tự động, sản phẩm của nó có thể được qPCR phát hiện trực tiếp.
Ứng dụng của UCOM
Ung thư phổi
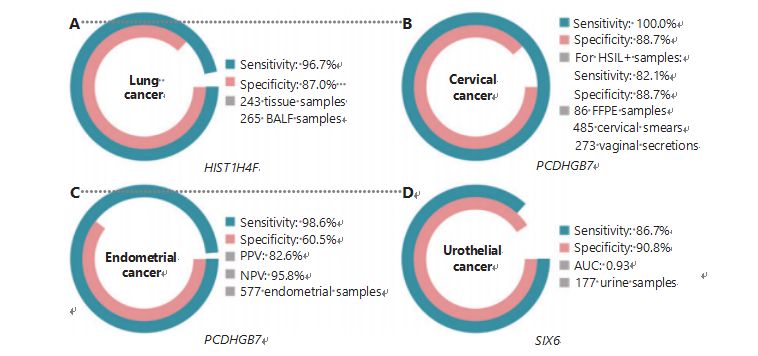
Ung thư phổi là loại ung thư được chẩn đoán thường xuyên thứ hai và gây tử vong nhiều nhất trên toàn thế giới, chiếm 11,4% số ca mắc mới và 18,0% số ca tử vong mới1.Trong số tất cả các chẩn đoán, 85% là ung thư phổi không phải tế bào nhỏ (NSCLC) và 15% là ung thư phổi tế bào nhỏ (SCLC), có mức độ ác tính cao hơn38.Chụp cắt lớp vi tính liều thấp (LDCT) là phương pháp sàng lọc được khuyến nghị hiện nay đối với bệnh ung thư phổi và đã được chứng minh là cải thiện khả năng phát hiện sớm và giảm tỷ lệ tử vong6;tuy nhiên, do độ đặc hiệu thấp và khả năng tiếp cận kém, LDCT vẫn chưa được coi là phương pháp sàng lọc thỏa đáng, cũng như các dấu hiệu ung thư phổ biến khác, chẳng hạn như CEA39.Chi phí và khả năng chẩn đoán bị bỏ sót và chẩn đoán sai trong chiến lược sàng lọc LDCT cản trở tiến trình thúc đẩy sàng lọc ung thư phổi40.HIST1H4F, một UCOM, có tiềm năng to lớn như một dấu ấn sinh học phát hiện sớm trong các mẫu dịch phế quản phế nang (BALF)27.HIST1H4F được tăng cường methyl hóa trong ung thư biểu mô tuyến phổi và ung thư biểu mô tế bào vảy phổi, với độ đặc hiệu phát hiện là 96,7% và độ nhạy là 87,0% (Hình 4A) và hiệu suất vượt trội đối với bệnh ung thư giai đoạn I27.HIST1H4F có độ đặc hiệu 96,5% và độ nhạy 85,4% đối với NSCLC, và 96,5% và 95,7% tương ứng đối với SCLC27.Ngoài ra, các mẫu của tám loại ung thư khác, bao gồm ung thư tuyến tụy và đại trực tràng, đã xác nhận rằng HIST1H4F bị tăng methyl hóa ở cả tám loại27.
Ung thư cổ tử cung
Ung thư cổ tử cung là loại ung thư được chẩn đoán thường xuyên thứ tư và là nguyên nhân gây tử vong do ung thư đứng thứ tư ở phụ nữ vào năm 2020, chiếm 3,1% số ca mắc mới và 3,4% số ca tử vong liên quan đến ung thư trên toàn cầu1.Để loại trừ ung thư cổ tử cung vào năm 2030, theo đề xuất của WHO, việc phát hiện sớm ung thư cổ tử cung là cần thiết.Nếu được phát hiện ở giai đoạn đầu, tỷ lệ sống sót sau 5 năm đạt tới 92% với ung thư cổ tử cung xâm lấn41.Hướng dẫn của Hiệp hội Ung thư Hoa Kỳ (ACS) đề xuất xét nghiệm tế bào cổ tử cung, xét nghiệm HPV sơ cấp hoặc xét nghiệm cotest để sàng lọc42.Tế bào cổ tử cung là phương pháp xâm lấn và chỉ có thể phát hiện được 63,5% trường hợp CIN2+37.
Ngược lại, PCDHGB7 đã hoạt động tốt hơn nhiều khi sử dụng phết tế bào Pap và dịch tiết âm đạo, đồng thời có thể phân biệt HSIL với LSIL một cách hiệu quả trong giai đoạn cực sớm.Riêng PCDHGB7 có độ nhạy 100,0% và độ đặc hiệu 88,7% đối với ung thư cổ tử cung (Hình 4B), độ nhạy 82,1% và độ đặc hiệu 88,7% đối với mẫu HSIL+30.PCDHGB7 cũng có độ nhạy 90,9% và độ đặc hiệu 90,4% trong các mẫu dịch tiết âm đạo đối với bệnh ung thư cổ tử cung, dễ thu thập hơn nhiều30.Khi kết hợp với xét nghiệm HPV (giờ) nguy cơ cao hoặc Xét nghiệm tế bào học Thinprep (TCT), PCDHGB7 có độ nhạy tăng lên 95,7% và độ đặc hiệu là 96,2%, vượt trội đáng kể so với xét nghiệm hrHPV (20,3%), TCT (51,2%). ) và cả hai kết hợp (57,8%) đối với ung thư cổ tử cung30.PCDHGB7 cũng đã được chứng minh là có khả năng tăng cường methyl hóa trong 17 loại ung thư từ cơ sở dữ liệu TCGA, cho thấy tính phù hợp của nó trong họ UCOM30.
Hình 4 UCOM đã được xác nhận trong bốn loại ung thư trong các nghiên cứu lâm sàng quy mô lớn.A. Hiệu suất của HIST1H4F, một UCOM, trong việc phát hiện ung thư phổi của 508 mẫu.B. Hiệu suất của PCDHGB7, một UCOM, trong việc phát hiện ung thư cổ tử cung của 844 mẫu.C. Hiệu suất của PCDHGB7, một UCOM, trong phát hiện ung thư nội mạc tử cung của 577 mẫu bàn chải Pap và Tao nội mạc tử cung.D. Hiệu suất của SIX6, một UCOM, trong việc phát hiện ung thư biểu mô đường tiết niệu của 177 mẫu.
EC
EC là một trong những bệnh ung thư hệ sinh sản nữ phổ biến nhất trên toàn thế giới, với ước tính khoảng 4,2 triệu ca mắc mới và 1% số ca tử vong liên quan đến ung thư hàng năm1.Với chẩn đoán thành công ở giai đoạn đầu, EC có thể chữa khỏi và có tỷ lệ sống sót sau 5 năm là 95% đối với bệnh ung thư giai đoạn I.Những bệnh nhân có triệu chứng, chẳng hạn như chảy máu tử cung bất thường, được đánh giá lâm sàng định kỳ và trải qua các thủ thuật sinh thiết xâm lấn và gây đau đớn, mặc dù cuối cùng chỉ có 5%–10% phát triển EC43.Siêu âm qua âm đạo, là phương pháp phát hiện phổ biến, rất không đáng tin cậy do không có khả năng phân biệt các thay đổi nội mạc tử cung lành tính với ác tính và tỷ lệ dương tính giả cao44.
Một so sánh song song giữa huyết thanh CA-125, dấu ấn sinh học EC được triển khai rộng rãi và PCDHGB7 đã được tiến hành.Huyết thanh CA-125 có độ nhạy 24,8%, điều này cho thấy CA-125 là dấu hiệu không đầy đủ cho EC mặc dù độ đặc hiệu là 92,3%31.Phát hiện PCDHGB7 bằng mẫu bàn chải Pap mang lại độ nhạy 80,65% và độ đặc hiệu 82,81% cho các giai đoạn ECatall, trong khi bàn chải Tao có độ nhạy 61,29% và độ đặc hiệu 95,31%31.Mô hình chẩn đoán PCDHGB7, dựa trên Me-qPCR, mang lại độ nhạy 98,61%, độ đặc hiệu 60,5% và độ chính xác tổng thể là 85,5%, sử dụng mẫu bàn chải Pap và Tao (Hình 4C)31.
Ung thư biểu mô tiết niệu
Ung thư biểu mô tiết niệu, bao gồm ung thư bàng quang, xương chậu thận và niệu quản, là loại ung thư được chẩn đoán thường xuyên thứ bảy vào năm 2020 trên toàn thế giới, gây ra 5,2% số ca mắc mới và 3,9% số ca tử vong1.Ung thư tiết niệu, hơn 50% trong số đó là ung thư bàng quang, là loại ung thư được chẩn đoán thường xuyên thứ tư ở Hoa Kỳ vào năm 2022, chiếm 11,6% số trường hợp mới được chẩn đoán3.Khoảng 75% bệnh ung thư bàng quang được phân loại là ung thư bàng quang xâm lấn không cơ, giới hạn ở niêm mạc hoặc lớp dưới niêm mạc45.Sinh thiết nội soi bàng quang là tiêu chuẩn vàng để chẩn đoán ung thư biểu mô tiết niệu được thực hiện bằng phương pháp lai huỳnh quang tại chỗ (FISH) và xét nghiệm tế bào học.FISH và tế bào học có hiệu suất chẩn đoán kém và nội soi bàng quang xâm lấn và có nguy cơ bỏ sót các tổn thương vi mô, hiểu sai các tổn thương và có khả năng gây lan rộng hoặc tái phát ung thư46.UCOM đã được xác nhận trước đây, PCDHGB7, cũng được chứng minh là có tính chất tăng methyl hóa trong ung thư biểu mô đường tiết niệu, với diện tích dưới đường cong là 0,86, cho thấy khả năng chẩn đoán tiềm năng30.Để xác nhận thêm nhiều UCOM hơn và phù hợp hơn với nhiều loại mẫu hơn, SIX6, một UCOM mới, đã được kiểm tra và cho thấy tiềm năng chẩn đoán tuyệt vời trong việc phát hiện sớm ung thư biểu mô đường tiết niệu bằng cách sử dụng mẫu nước tiểu trên nền tảng Me-qPCR.Việc phát hiện SIX6 bằng cách sử dụng mẫu nước tiểu cho thấy độ nhạy cạnh tranh là 86,7% và độ đặc hiệu là 90,8% (Hình 4D), đồng thời không xâm lấn và dễ dàng thu được32.Tiềm năng của SIX6 trong việc theo dõi di căn và đánh giá hiệu quả điều trị hiện đang được nghiên cứu.
Tương lai và những thách thức
UCOM có hiệu suất mạnh mẽ trong khả năng chẩn đoán nhiều bệnh ung thư, nhưng vẫn còn nhiều việc phải làm.Chúng tôi đã mở rộng danh sách UCOM và tích cực xác nhận UCOM trong nhiều loại ung thư hơn, bao gồm cả những loại ung thư khó phát hiện theo truyền thống.Kết quả xác nhận từ cơ sở dữ liệu TCGA đã chứng thực thêm việc ứng dụng UCOM trong nhiều loại ung thư hơn và nhiều tình huống hơn.Trong một cuộc điều tra sơ bộ, UCOM đã được chứng minh là có tiềm năng chẩn đoán mạnh mẽ đối với ung thư đường mật và ung thư biểu mô tuyến tụy, gần như không thể chẩn đoán ở giai đoạn đầu bằng các phương pháp sàng lọc hiện tại32,47.Khả năng phát hiện các bệnh ung thư hiếm gặp bằng UCOM có thể được sử dụng với DNA khối u đang lưu hành (ctDNA) bằng nền tảng sinh thiết lỏng cải tiến48.Một nghiên cứu liên quan đến bảng phát hiện ung thư toàn thể dựa trên DNA huyết tương mang lại độ nhạy 57,9%49.Mặc dù có độ đặc hiệu cao nhưng hiệu suất tổng thể cho thấy vẫn còn chỗ cần cải thiện.
Các đặc điểm độc đáo của UCOM cũng đã hỗ trợ việc điều tra tiềm năng của UCOM trong đánh giá hiệu quả điều trị và theo dõi tái phát.Theo Tiêu chí đánh giá đáp ứng ở khối u rắn (RECIST), hình ảnh y tế là phương pháp được khuyến nghị để theo dõi tái phát và đánh giá hiệu quả điều trị, trong khi các dấu hiệu khối u được sử dụng riêng lẻ để đánh giá50.Tuy nhiên, trên thực tế, các phương pháp chẩn đoán hình ảnh bị ảnh hưởng rất nhiều bởi tần suất và thời gian, do đó khiến bệnh nhân gặp rủi ro và chi phí cao hơn51,52.SIX6 đã được xác nhận để đóng vai trò là yếu tố dự báo di căn của ung thư vú32.Giám sát ctDNA dựa trên sinh thiết lỏng cho phép giám sát theo thời gian thực đối với số tháng bệnh còn sót lại ở mức tối thiểu trước khi phát hiện bằng X quang, lý tưởng nhất là trì hoãn và ngăn ngừa sự tiến triển của ung thư liên quan đến tái phát53.Kết quả sơ bộ cho thấy UCOM phản ánh mức độ tăng methyl hóa ung thư trong thời gian thực ngay sau phẫu thuật và điều trị32.Độ nhạy cao được thể hiện bởi UCOM và khả năng ứng dụng trong nhiều loại mẫu không xâm lấn cho phép UCOM đóng vai trò là dấu ấn sinh học theo dõi tái phát chính xác trong khi vẫn duy trì sự tuân thủ cao của bệnh nhân.
Đồng thời, khả năng tiếp cận công chúng với bài kiểm tra là một vấn đề lớn khác cần nỗ lực nhiều hơn.Trong khi sự hợp tác phát hiện UCOM đã được áp dụng ở nhiều bệnh viện hơn với hy vọng mang lại lợi ích cho nhiều bệnh nhân hơn, thì việc phát hiện và sàng lọc chuyên nghiệp đã được thực hiện tích cực ở vùng nông thôn Trung Quốc.UCOM yêu cầu khả năng tiếp cận được cải thiện để đủ điều kiện trở thành công cụ sàng lọc khả thi, đặc biệt đối với các khu vực kém phát triển.
Mặc dù ứng dụng UCOM mang lại kết quả phát hiện sớm đầy hứa hẹn nhưng vẫn tồn tại nhiều điều chưa biết về UCOM.Với việc thăm dò tích cực, cần có nghiên cứu bổ sung về lý do tại sao UCOM hiện diện phổ biến trong các bệnh ung thư.Các cơ chế điều hòa biểu sinh cơ bản của UCOM rất đáng được nghiên cứu thêm, điều này có thể chứng minh một hướng đi mới trong điều trị ung thư.Quay trở lại mối tương tác giữa tính đồng nhất và tính không đồng nhất của khối u, chúng tôi quan tâm đến lý do tại sao UCOM có thể là một ngoại lệ đối với phần lớn các dấu hiệu sinh học ung thư có liên quan chặt chẽ với các loại ung thư cụ thể.Vai trò của quang sai methyl hóa DNA do UCOM xác định trong nguyên nhân khối u, sự tiến triển của khối u và di căn chưa được xác định trong quá trình mất và lấy lại nhận dạng tế bào và cần phải kiểm tra kỹ lưỡng.Một mối quan tâm lớn khác nằm ở phạm vi kết hợp đặc điểm đồng nhất của UCOM với các dấu hiệu duy nhất của mô với hy vọng tiếp cận việc phát hiện chính xác dấu vết ung thư và xác định nguồn gốc mô khối u theo cách ngược lại.UCOM có thể trở thành công cụ lý tưởng để ngăn ngừa ung thư, phát hiện ung thư và có khả năng bảo vệ và loại bỏ ung thư.
Cấp hỗ trợ
Công trình này được hỗ trợ bởi Chương trình R&D trọng điểm quốc gia của Trung Quốc (Số tài trợ 2022BEG01003), Quỹ khoa học tự nhiên quốc gia Trung Quốc (Số tài trợ 32270645 và 32000505), Tài trợ từ Ủy ban y tế tỉnh Hắc Long Giang (Số tài trợ 2020-111) và một khoản tài trợ từ Viện Khoa học và Công nghệ Heze (Số tài trợ 2021KJPT07).
Xung đột về tuyên bố lãi suất
Wei Li là Giám đốc R&D của Công ty TNHH Công nghệ sinh học Epiprobe Thượng Hải. Wenqiang Yu phục vụ trong Ban cố vấn khoa học của Epiprobe.W. Yu và Epiprobe đã phê duyệt các bằng sáng chế đang chờ xử lý liên quan đến công việc này.Tất cả các tác giả khác tuyên bố không có lợi ích cạnh tranh.
Sự đóng góp của tác giả
Lên ý tưởng và thiết kế dự án: Chengchen Qian và Wenqiang Yu.
Người viết bài báo: Chengchen Qian.
Thực hiện các minh họa: Chengchen Qian.
Xem xét và chỉnh sửa bản thảo: Xiaolong Zou, Wei Li, Yinshan Li và Wenqiang Yu.
Người giới thiệu
1. Sung H, Ferlay J, Siegel RL, LaversanneM, Soerjomataram I, Jemal A, et al.Thống kê Ung thư Toàn cầu 2020: Ước tính của GLOBOCAN về
tỷ lệ mắc và tử vong trên toàn thế giới đối với 36 bệnh ung thư ở 185 quốc gia.Phòng khám Ung thư CA J.2021;71: 209-49.
2. Xia C, Dong X, Li H, Cao M, Sun D, He S, et al.Thống kê về ung thư ở Trung Quốc và Hoa Kỳ, 2022: hồ sơ, xu hướng và yếu tố quyết định.Chin MedJ (Tiếng Anh).2022;135: 584-90.
3. Siegel RL, Miller KD, WagleNS, JemalA.Thống kê về ung thư, 2023. CA Cancer J Clinic.2023;73: 17-48.
4. Crosby D, BhatiaS, Brindle KM, Coussens LM, Dive C, Emberton M, et al.Phát hiện sớm ung thư.Khoa học.2022;375: eaay9040.
5. Ladabaum U, Dominitz JA, KahiC, Schoen RE.Chiến lược dành cho
sàng lọc ung thư đại trực tràng.Khoa tiêu hóa.2020;158: 418-32.
6. Tanoue LT, Tanner NT, Gould MK, Silvestri GA.Sàng lọc ung thư phổi.Am J Respir Crit Care Med.2015;191: 19-33.
7. Bouvard V, WentzensenN, Mackie A, Berkhof J, BrothertonJ, Giorgi-Rossi P, và những người khác.Quan điểm của IARC về sàng lọc ung thư cổ tử cung.N EnglJ Med.2021;385: 1908-18.
8. Xue P, Ng MTA, QiaoY.Những thách thức của soi cổ tử cung trong sàng lọc ung thư cổ tử cung ở LMIC và các giải pháp bằng trí tuệ nhân tạo.BMC Med.2020;18: 169.
9. Johnson P, Chu Q, Đào DY, Lộ YMD.Dấu ấn sinh học lưu hành trong chẩn đoán và quản lý ung thư biểu mô tế bào gan.Nat Rev Gastroenterol Hepatol.2022;19: 670-81.
10. Van PoppelH, Albreht T, Basu P, HogenhoutR, CollenS, Roobol M. Phát hiện sớm ung thư tuyến tiền liệt dựa trên PSA ở Châu Âu và trên toàn cầu: quá khứ, hiện tại và tương lai.Nat Rev Urol.2022;19:
562-72.
11. HolyoakeA, O'Sullivan P, Pollock R, Best T, Watanabe J, KajitaY,
et al.Phát triển xét nghiệm nước tiểu RNA đa kênh để phát hiện và phân tầng ung thư biểu mô tế bào chuyển tiếp của bàng quang.Ung thư lâm sàng Res.2008;14: 742-9.
12. Feinberg AP, Vogelstein B. Hypomethylation phân biệt gen của một số bệnh ung thư ở người với các gen bình thường của chúng.Thiên nhiên.1983;301: 89-92.
13. Ng JM, Yu J. Promoter tăng cường methyl hóa các gen ức chế khối u như là dấu ấn sinh học tiềm năng trong ung thư đại trực tràng.Khoa học IntJ Mol.2015;16: 2472-96.
14. Esteller M. Biểu sinh ung thư: methylome DNA và bản đồ sửa đổi histone.Nat Rev Genet.2007;8: 286-98.
15. Nishiyama A, Nakanishi M. Điều hướng bối cảnh methyl hóa DNA của bệnh ung thư.Xu hướng Genet.2021;37: 1012-27.
16. Xie W, Schultz MD, ListerR, Hou Z, Rajagopal N, Ray P, và cộng sự.Phân tích biểu sinh về sự biệt hóa đa dòng của tế bào gốc phôi người.Tế bào.2013;153: 1134-48.
17. Li Y, Zheng H, Wang Q, Chu C, WeiL, Liu X, et al.Các phân tích trên toàn bộ bộ gen cho thấy vai trò của Polycomb trong việc thúc đẩy quá trình giảm oxy hóa của các thung lũng methyl hóa DNA.Bộ gen Biol.2018;19: 18.
18. Koch A, JoostenSC, Feng Z, de Ruijter TC, DrahtMX, MelotteV,
et al.Phân tích quá trình methyl hóa DNA trong bệnh ung thư: xem xét lại vị trí.Nat Rev Clinic Oncol.2018;15: 459-66.
19. KleinEA, Richards D, Cohn A, TummalaM, Lapham R, Cosgrove D, và cộng sự.Xác nhận lâm sàng của xét nghiệm phát hiện sớm đa ung thư dựa trên quá trình methyl hóa có mục tiêu bằng cách sử dụng bộ xác nhận độc lập.Ann Oncol.2021;32: 1167-77.
20. Hanahan D, Weinberg RA.Dấu hiệu của bệnh ung thư.Tế bào.2000;100: 57-70.
21. Hanahan D. Dấu hiệu của bệnh ung thư: những khía cạnh mới.Ung thư Discov.2022;12: 31-46.
22. Schwartzberg L, Kim ES, Liu D, Schrag D. Ung thư chính xác: ai, như thế nào, cái gì, khi nào và khi nào không?Sách giáo dục Oncol của Am Sóc Clinic.2017: 160-9.
23. Liu H, Meng X, Wang J. Quá trình methyl hóa định lượng theo thời gian thực
Phát hiện gen PAX1 trong sàng lọc ung thư cổ tử cung.Ung thư phụ khoa IntJ.2020;30: 1488-92.
24. Imperiale TF, RansohoffDF, Itzkowitz SH, Levin TR, Lavin P, Lidgard GP, và những người khác.Xét nghiệm DNA đa mục tiêu để sàng lọc ung thư đại trực tràng.N EnglJ Med.2014;370: 1287-97.
25. Li J, Li Y, Li W, Luo H, Xi Y, Dong S, et al.Hướng dẫn định vị
giải trình tự xác định các kiểu methyl hóa DNA bất thường làm thay đổi nhận dạng tế bào và mạng lưới giám sát miễn dịch khối u.bộ gen
Res.2019;29: 270-80.
26. Gao Q, LinYP, Li BS, Wang GQ, Dong LQ, Shen BY, et al.Phát hiện đa ung thư không xâm lấn bằng cách tuần hoàn trình tự methyl hóa DNA không có tế bào (THUNDER): nghiên cứu phát triển và xác nhận độc lập.Ann Oncol.2023;34: 486-95.
27. Dong S, Li W, Wang L, Hu J, Song Y, Zhang B, et al.Các gen liên quan đến histone bị hypermethylated trong ung thư phổi và hypermethylated
HIST1H4F có thể đóng vai trò là dấu ấn sinh học cho bệnh ung thư.Ung thư Res.2019;79: 6101-12.
28. HeijnsdijkEA, Wever EM,AuvinenA, Hugosson J, Ciatto S, Nelen V, et al.Ảnh hưởng chất lượng cuộc sống của sàng lọc kháng nguyên đặc hiệu tuyến tiền liệt.N EnglJ Med.2012;367: 595-605.
29. LuzakA, Schnell-Inderst P, Bühn S, Mayer-Zitarosa A, Siebert U. Hiệu quả lâm sàng của các xét nghiệm dấu ấn sinh học sàng lọc ung thư được cung cấp dưới dạng dịch vụ y tế tự chi trả: đánh giá có hệ thống.Y tế công cộng Eur J.2016;26: 498-505.
30. Dong S, Lu Q,Xu P, Chen L, Duẩn X, Mao Z, et al.
PCDHGB7 được tăng cường methyl hóa như một chất đánh dấu ung thư phổ biến và ứng dụng của nó trong sàng lọc ung thư cổ tử cung sớm.Lâm sàng dịch Med.2021;11: e457.
31. Yuan J, Mao Z, Lu Q,Xu P, Wang C, Xu X, et al.PCDHGB7 được tăng cường methyl hóa như một dấu ấn sinh học để phát hiện sớm ung thư nội mạc tử cung trong các mẫu bàn chải nội mạc tử cung và các vết xước cổ tử cung.Front Mol Biosci.2022;8: 774215.
32. Dong S, Yang Z,Xu P, Zheng W, Zhang B, Fu F, et al.Hỗ trợ
sửa đổi biểu sinh độc quyền trên SIX6 với quá trình tăng cường methyl hóa cho giai đoạn tiền ung thư và theo dõi sự xuất hiện di căn.Mục tiêu truyền tín hiệu ở đó.2022;7: 208.
33. Huang L, Guo Z, Wang F, Fu L. Đột biến KRAS: từ không thể điều trị được đến có thể điều trị được trong bệnh ung thư.Mục tiêu truyền tín hiệu ở đó.2021;6: 386.
34. Belinsky SA, Nikula KJ, PalmisanoWA, MichelsR, SaccomannoG, GabrielsonE, và cộng sự.Quá trình methyl hóa mạnh mẽ p16 (INK4a) là sự kiện sớm xảy ra trong bệnh ung thư phổi và là dấu ấn sinh học tiềm năng để chẩn đoán sớm.Proc Natl Acad Sci U SA.1998;95: 11891-6.
35. Robertson KD.Quá trình methyl hóa DNA và bệnh tật ở người.Nat Rev Genet.2005;6: 597-610.
36. WentzensenN, Walker JL, Gold MA, Smith KM, ZunaRE,
Mathews C và cộng sự.Nhiều sinh thiết và phát hiện tiền thân ung thư cổ tử cung khi soi cổ tử cung.J lâm sàng Oncol.2015;33: 83-9.
37. De Strooper LM, Meijer CJ, Berkhof J, Hesselink AT, Snijders
PJ, Steenbergen RD, và cộng sự.Phân tích methyl hóa FAM19A4
gen trong vết xước cổ tử cung có hiệu quả cao trong việc phát hiện cổ tử cung
ung thư biểu mô và tổn thương CIN2/3 tiến triển.Ung thư Trước Res (Phila).2014;7: 1251-7.
38. AA Thái Lan, Solomon BJ, Sequist LV, Gainor JF, Heist RS.Ung thư phổi.Lancet.2021;398: 535-54.
39. Grunnet M, Sorensen JB.Kháng nguyên carcinoembryonic (CEA) là dấu hiệu khối u trong ung thư phổi.Ung thư phổi.2012;76: 138-43.
40. Gỗ DE, KazerooniEA, Baum SL, EapenGA, EttingerDS, Hou L, et al.Sàng lọc Ung thư Phổi, Phiên bản 3.2018, Hướng dẫn Thực hành Lâm sàng NCCN trong Ung thư.J Natl Compr Canc Netw.2018;16: 412-41.
41. Hiệp hội Ung thư Hoa Kỳ.Sự thật và số liệu về ung thư.Atlanta, GA, Hoa Kỳ: Hiệp hội Ung thư Hoa Kỳ;2023 [cập nhật 2023 ngày 1 tháng 3;trích dẫn 2023 ngày 22 tháng 8].
42. FonthamETH, Wolf AMD, Church TR, EtzioniR, Flowers CR,
Herzig A, và cộng sự.Sàng lọc ung thư cổ tử cung cho những người có nguy cơ trung bình: Cập nhật hướng dẫn năm 2020 của Hiệp hội Ung thư Hoa Kỳ.Phòng khám Ung thư CA J.2020;70: 321-46.
43. Clarke MA, Long BJ, Del Mar MorilloA, Arbyn M, Bakkum-Gamez JN, Wentzensen N. Mối liên quan giữa nguy cơ ung thư nội mạc tử cung với chảy máu sau mãn kinh ở phụ nữ: tổng quan hệ thống và phân tích tổng hợp.JAMA Thực tập sinh Med.2018;178: 1210-22.
44. Jacobs I, Gentry-MaharajA, Burnell M, ManchandaR, Singh N,
Sharma A và cộng sự.Độ nhạy của sàng lọc siêu âm qua âm đạo
đối với ung thư nội mạc tử cung ở phụ nữ sau mãn kinh: một nghiên cứu bệnh chứng trong đoàn hệ UKCTOCS.Lancet Oncol.2011;12: 38-48.
45. BabjukM, Burger M, CompératEM, Gontero P, MostafidAH,
PalouJ và cộng sự.Hướng dẫn của Hiệp hội Tiết niệu Châu Âu về Ung thư bàng quang không xâm lấn cơ (TaT1 và Ung thư biểu mô tại chỗ) -
Cập nhật 2019.Euro Urol.2019;76: 639-57.
46. Aragon-Ching JB.Những thách thức và tiến bộ trong chẩn đoán, sinh học và điều trị ung thư biểu mô đường tiết niệu trên và bàng quang.Urol Oncol.2017;35: 462-4.
47. Rizvi S, KhanSA, Hallemeier CL, Kelley RK, Gores GJ.
Ung thư đường mật – phát triển các khái niệm và chiến lược điều trị.Nat Rev Clinic Oncol.2018;15: 95-111.
48. Ye Q, Ling S, Zheng S, Xu X. Sinh thiết lỏng trong tế bào gan
ung thư biểu mô: tế bào khối u lưu hành và DNA khối u lưu hành.Ung thư Mol.2019;18: 114.
49. Zhang Y, Yao Y, Xu Y, Li L, Gong Y, Zhang K, et al.ung thư toàn thể
Phát hiện DNA khối u lưu hành ở hơn 10.000 bệnh nhân Trung Quốc.Xã Nat.2021;12: 11.
50. Eisenhauer EA, Therasse P, BogaertsJ, Schwartz LH, Sargent D, Ford R, và cộng sự.Tiêu chí đánh giá phản ứng mới trong khối u rắn: hướng dẫn RECIST sửa đổi (phiên bản 1.1).Ung thư Eur J.2009;45: 228-47.
51. LitièreS, Collette S, de Vries EG, Seymour L, BogaertsJ.RECIST - học từ quá khứ để xây dựng tương lai.Nat Rev Clinic Oncol.
2017;14: 187-92.
52. Seymour L, BogaertsJ, Perrone A, FordR, Schwartz LH, Mandrekar S, và cộng sự.iRECIST: hướng dẫn về tiêu chí đáp ứng để sử dụng trong các thử nghiệm
thử nghiệm liệu pháp miễn dịch.Lancet Oncol.2017;18: e143-52.
53. PantelK, Alix-Panabières C. Sinh thiết lỏng và bệnh còn sót lại tối thiểu – những tiến bộ mới nhất và ý nghĩa trong việc chữa trị.Nat Rev Clinic Oncol.2019;16: 409-24.
Trích dẫn bài viết này là: Qian C, Zou X, Li W, Li Y, Yu W. Tiền đồn chống lại bệnh ung thư: các dấu hiệu ung thư phổ quát.Ung thư Biol Med.2023;20: 806-815.
doi: 10.20892/j.issn.2095-3941.2023.0313
Thời gian đăng: May-07-2024